Kurzbeschrieb
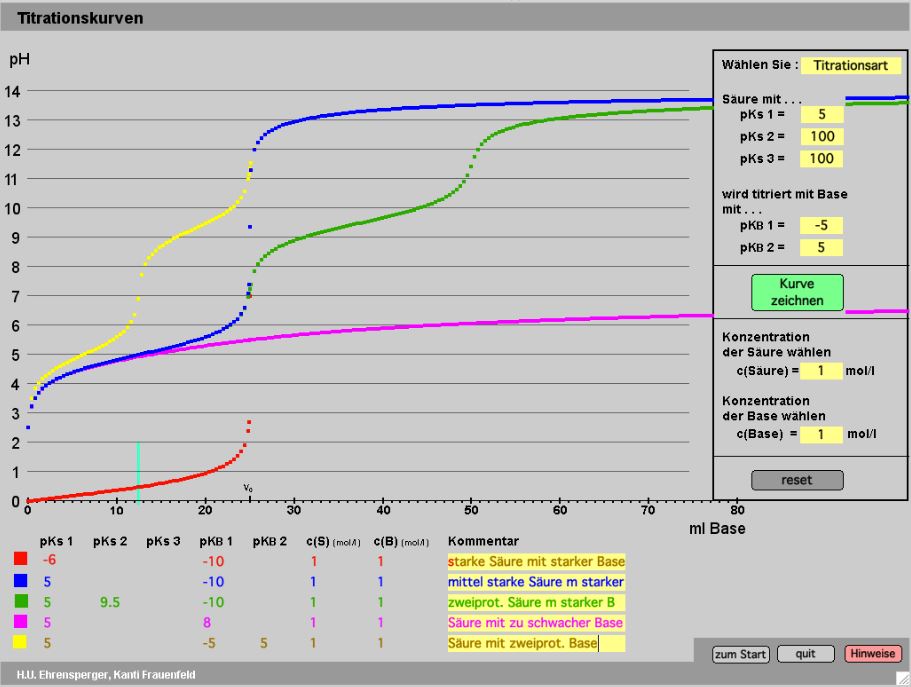
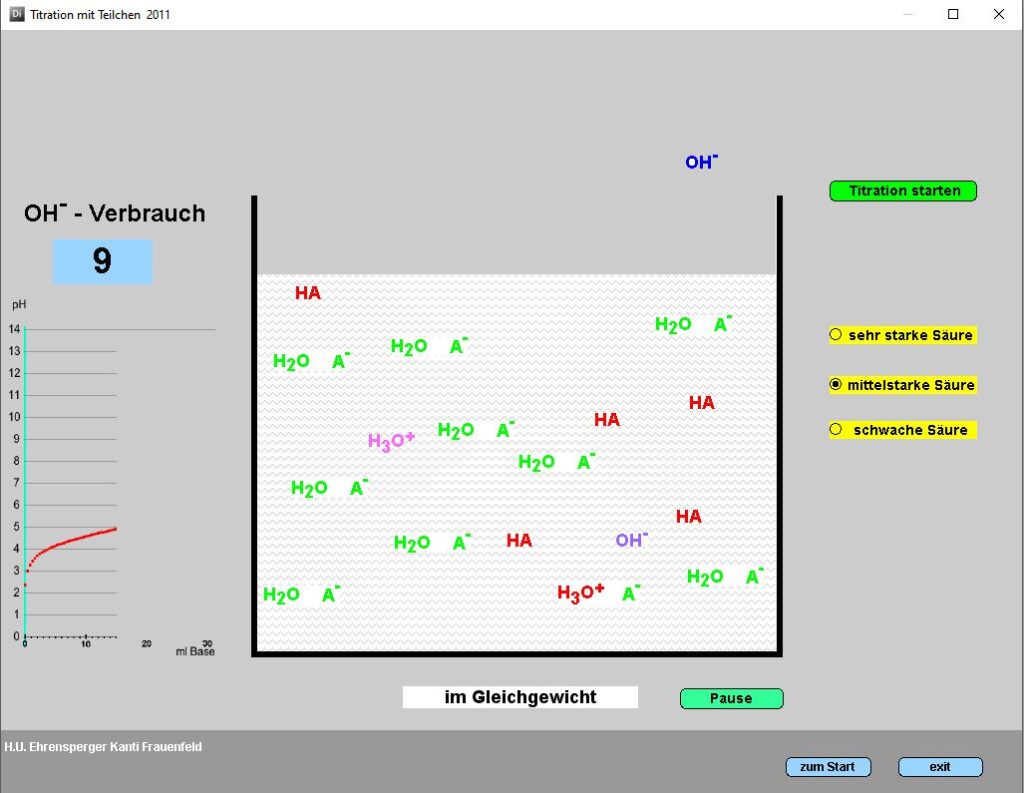
Zeigt schematisch das Prinzip der Titration für Säuren unterschiedlicher Säurestärke.
Einsatz im Unterricht
Als Einstieg zur Erklärung der Titration. Zeigt, dass Titration eigentlich ein «chemisches Abzählen» ist und dass der Titrationsendpunkt nicht immer bei pH = 7 gewählt werden kann.
Hinweis
OH– reagiert in der Darstellung nicht nur mit H3O+, sondern auch mit der protonierten Form der Säure. Für „Puristen“ sei der Hinweis gestattet,
dass H3O+ bei pH 5 zwar immer noch die
stärkste Säure ist, aber in über 33’000 mal
kleinerer Konzentration vorkommt als z.B.
das Essigsäuremolekül in einer Essigsäurelösung mit c(HAc) = 1 mol/l.